Mindentudó mikroglia
A gyulladás normális esetben egy jól szabályozott folyamat, amely azt a célt szolgálja, hogy a kórokozót mielőbb eltakaríthassa a szervezet, vagy hogy segítse a sérült szövetek regenerációját. Hétköznapi példa a gyulladásra, amikor megvágjuk a kezünket. Bepirosodik, megduzzad, fáj, nem tudjuk behajlítani az ujjunkat. Ezek a klasszikus tünetek azért jelentkeznek, mert a szöveti sérülés – hasonlóan a fertőzéshez – olyan folyamatokat indít el, amelyek nagyon hamar odavonzzák a környező fehérvérsejteket. Olyan anyagok is termelődnek, amelyek fokozzák a helyi erek átjárhatóságát számos fehérje számára, és segítik a kórokozók eliminálását, a sérült szövet eltávolítását. Gyulladáshoz egyébként vágás és felületi sérülés sem kell. A torokgyulladásnál a nyálkahártyán és a nyirokcsomókban „őrjáratozó” immunsejtek érzékelik a kórokozók jelenlétét, ami ellen az immunrendszer fellép.
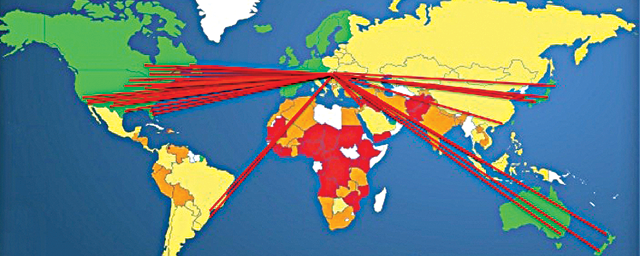
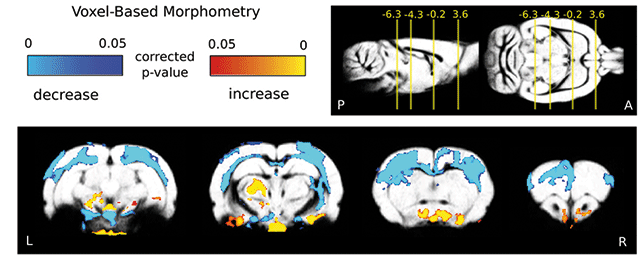
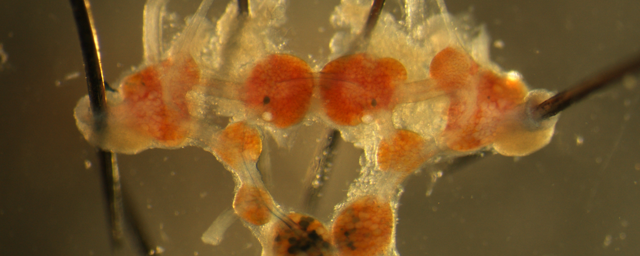
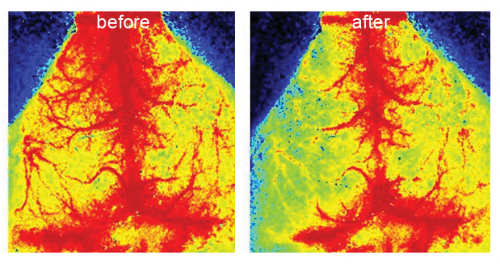 A gyulladásos folyamatok modulálják az agyi vérkeringés átrendeződését átmeneti érelzáródást követően (laser speckle contrast imaging [az agyi vérkeringés valós idejű vizsgálatára alkalmas képalkotó módszer])
A gyulladásos folyamatok modulálják az agyi vérkeringés átrendeződését átmeneti érelzáródást követően (laser speckle contrast imaging [az agyi vérkeringés valós idejű vizsgálatára alkalmas képalkotó módszer])Az idegrendszerben ez annyiban komplexebb, hogy itt normál esetben nem jelenhetnek meg nagy számban a szervezet egyéb területein – bőrben, tüdőben, belekben – fellelhető immunsejtek. Nem juthatnak az agyba, a gerincvelőbe – a vér-agy gát egyik feladata éppen ezek szabad mozgásának és a vérplazma beáramlásának a megakadályozása. Nem lenne ugyanis szerencsés, ha az agyi keringés dinamikája vagy a folyadékterek mérete, összetétele például a bőrhöz hasonló intenzitással változna, mert akkor számos idegrendszeri funkció nem működne. Az sem vezetne jóra, ha az immunsejtek akadálytalanul őrjáratoznának, mert az idegszövetben maradandó sérüléseket okozhatnának.
Az agy esetében kétféle különböző eredetű gyulladásról beszélhetünk. Sztrók vagy baleset okozta agyi trauma esetén maga az agyszövet sérül, ilyenkor annak gyulladásos sejtjei, a mikroglia sejtek hasonló gyulladásos fehérjéket termelnek, mint amilyeneket a bőrsérülés vagy a torokgyulladás esetén a fehérvérsejtek állítanak elő. Néhány éve ismerték fel, hogy ha gátoljuk azokat a kulcsfontosságú gyulladásos folyamatokat, amelyek alapvetően szerencsések egy periferiális szervben a baktériumok elleni védekezésben, akkor ezzel olyan esetben is csökkenthetjük az agyi sérülést, amikor a primer sérülés kvázi steril. (Leegyszerűsítve: steril sérülésnek – nem csak az agyban – azt az esetet nevezzük, amikor a primer sérülés nem kórokozók jelenlétében történik, például egy érelzáródás miatt az adott agyterület nem kap vért, és ez számos idegsejt halálához vezet.)
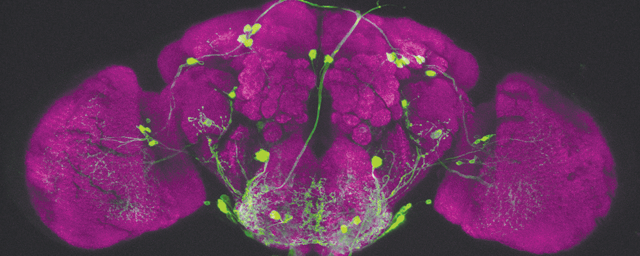
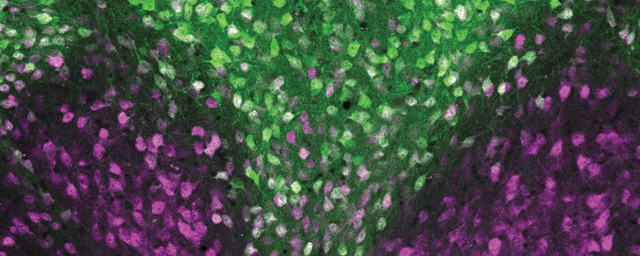
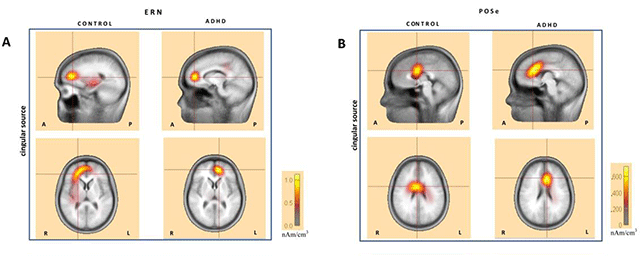
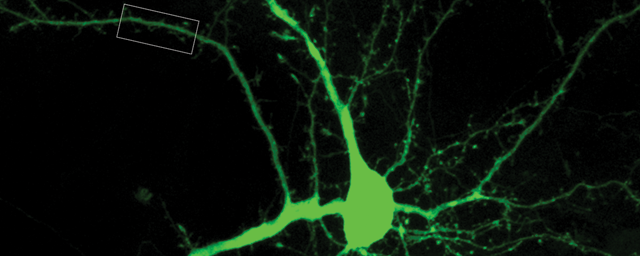
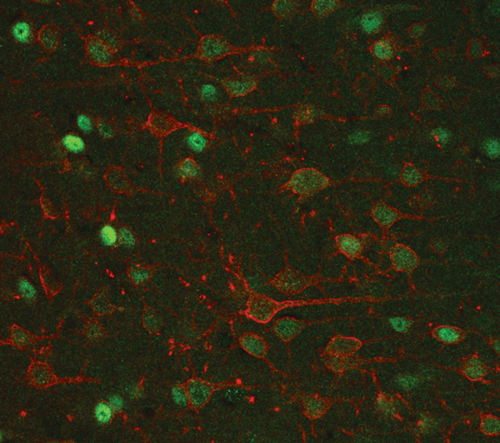 Aktív idegsejtek az agykéregben, agyi sérülés után.
Aktív idegsejtek az agykéregben, agyi sérülés után.Gyulladásos folyamatok kialakulhatnak az agyban krónikus vagy szisztémás gyulladás hatására is. A cukorbetegség, az érelmeszesedés, a magas vérnyomás különböző szervekben és ezek ereiben gyulladást indukál. Ha a gyulladás nagyon sok szervben egyszerre van jelen (gyakran hosszú ideig), akkor krónikus, esetenként sok szervre kiterjedő, szisztémás gyulladás épül fel, amiről tudjuk, hogy akkor is eléri az agy mikroglia sejtjeit, ha az agyban egyébként nem történt sérülés. Ha beüt a krach, például sztrók alakul ki, az ilyen agy teljesen másként reagál az akut sérülésre, mint egy fiatal, egészséges szervezet, ahol nincs jelen krónikus gyulladás. Ismert, hogy a perifériákon létrejövő krónikus gyulladásos betegségek szoros kapcsolatot mutatnak az idegrendszeri betegségek kialakulásával. A szakemberek véleménye szerint a modern korban megannyi krónikus betegséggel élünk együtt, ami számos idegrendszeri betegség okozója is lehet, hiszen a megváltozott életmóddal és a hosszú élettel párhuzamosan igen sok elváltozás dominanciája és hatása is megváltozik.
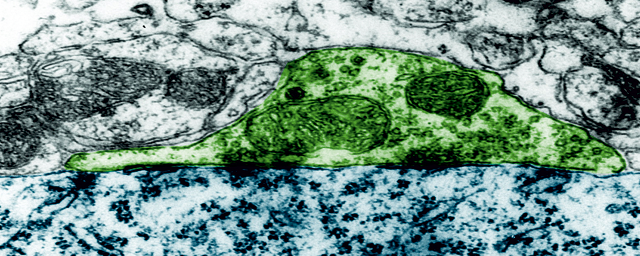
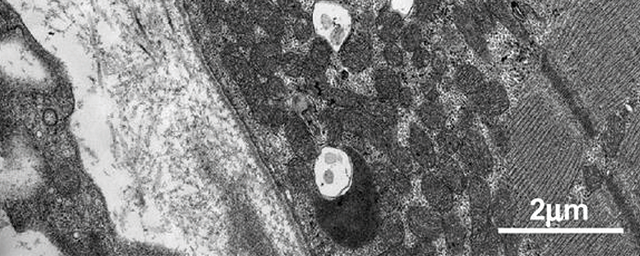
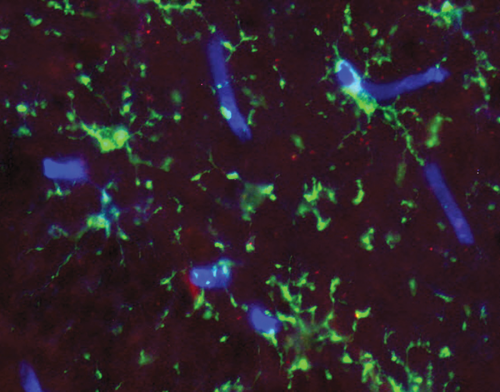 Krónikusan aktiválódott mikroglia sejtek kapcsolata agyi kapillárisokkal a szisztémás gyulladás egyik állatmodelljében.
Krónikusan aktiválódott mikroglia sejtek kapcsolata agyi kapillárisokkal a szisztémás gyulladás egyik állatmodelljében.„Mi azt szeretnénk megérteni, hogy a gyulladások miként hatnak az idegrendszeri patológiás folyamatokra. Ahhoz, hogy ez sikerüljön, vissza kell térnünk az alapmechanizmusokhoz. Fel kell tárni, hogy egy mikroglia sejt hogyan beszélget az idegsejtekkel, melyek azok a gyulladásos folyamatok, amelyek egy steril agyi sérülés hatására elindulnak, és hogyan válaszol erre az idegrendszer. Ha mindezt megértjük, találhatunk ígéretes támadáspontokat, ahol beavatkozhatunk” – vázolta az MTA Kísérleti Orvostudományi Kutatóintézetben működő csoportjának feladatait Dénes Ádám. A cél érdekében a Manchester Egyetemmel együtt a szisztémás krónikus gyulladás számos állatmodelljét is vizsgálták – kövér vagy éppen érelmeszesedett állatokat hoztak létre. Ezeknél ugyanúgy súlyosabb következményekkel járt a sztrók, mint az emberek esetében. Kutatásaik során rájöttek arra, hogy ezeket a hatásokat a gyulladásos folyamatok gátlásával csökkenteni lehet. Ez azt jelzi, hogy ezek a folyamatok megágyaznak számos idegrendszeri betegségnek, de éppen ezért be is avatkozhatunk, ha pontosan tudjuk, hogy hol lehet belenyúlni ebbe a rendszerbe.
Az állatkísérletek biztatóak, ám az itt kapott eredményeket nem lehet rögtön embereken alkalmazni – részben azért, mert a betegek életkoruk, genetikai hátterük és számos különféle betegségük miatt nagyfokú heterogenitást mutatnak. Nem véletlen, hogy korábban számos klinikai próba elbukott az idegrendszeri betegségek terén. Dénes Ádám szerint ezek zöme azért nem járt sikerrel, mert a céljuk az idegsejt sérülésének a kivédése volt. Hiába védjük meg azonban az idegsejtet a káros folyamatoktól, ha a mikrokörnyezet nem segíti azok életben maradását. Azt remélik, hogy a folyamatok jobb megértése pontosabb, hatékonyabb beavatkozást tesz majd lehetővé. Ma már ismernek olyan speciális támadáspontokat, ahol reményeik szerint a sztrók, az epilepszia, az Alzheimer- és a Parkinson-kór esetén segíthetik az idegsejtek túlélését. Könnyebb ugyanis megvédeni ezeket a sejteket, mint pótolni őket, ezért célszerűbbnek tűnik a kiváltó okok megértése és kezelése, mint megpróbálni „visszahozni a sírból” a sérült idegsejteket. Egy felnőtt agyat újrahuzalozni a rendszer komplexitása miatt rendkívül nehéznek látszik.
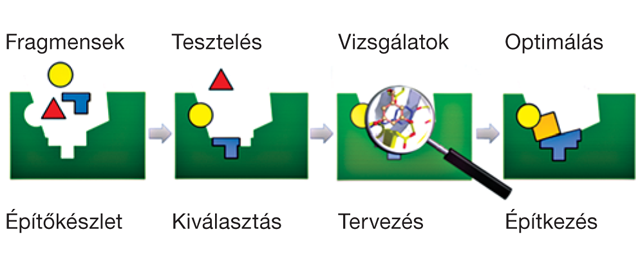
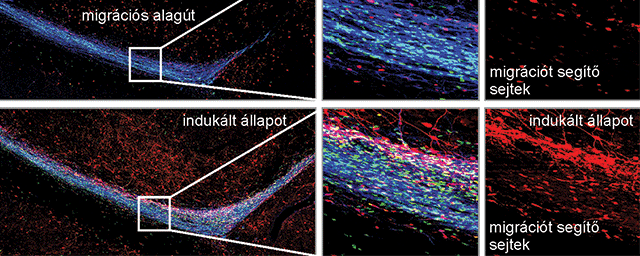
 Mikroglia-idegsejt kapcsolatok az emberi agyban.
Mikroglia-idegsejt kapcsolatok az emberi agyban.„E folyamatok vizsgálatára részben a Nemzeti Agykutatási Programból, a NAP-ból kapott támogatásnak köszönhetően olyan kutatómunka indulhatott el, amely nagyon értékes publikációkhoz vezetett, illetve ennek köszönhetően újabb kutatási támogatásokhoz jutottunk. A Lendület pályázat mellett az Európai Kutatási Tanács, az ERC pályázatát is sikerült így elnyernünk” – összegez a Manchesterből 2012-ben hazatért kutató, aki a NAP-os négy év legfontosabb eredményének egy olyan új kapcsolat felfedezését tartja, amely az idegsejtek és a mikroglia együttműködésének további megértését segítheti. Ez a kapcsolat véleményük szerint nagyon sok idegrendszeri betegségben játszhat fontos szerepet.•
2017. december