Őssejtkutatás: óriási a verseny
„Először azt kell tisztáznunk, hogy mit nevezünk őssejtnek” – figyelmeztet Sarkadi Balázs akadémikus, a Magyar Tudományos Akadémia Természettudományi Kutatóközpont Enzimológiai Intézetének professzora. Tág fogalomról van szó, amelybe az őssejtek két nagy csoportja, a szöveti és az embrionális őssejtek tartoznak.
Az új élet fogantatásakor a megtermékenyült petesejt osztódni kezd, a petevezetékben a méh felé vándorol, majd elérve azt beágyazódik a méhnyálkahártyába. A nyolcsejtes embrió még „mindentudó” (totipotens) sejtekből áll, amelyek mindegyike a felnőtt szervezet még bármilyen sejttípusává fejlődhet. A beágyazódó embrió később kialakuló embriócsomójából választhatjuk ki a „pluripotens” embrionális őssejteket, és így hozhatunk létre folyamatosan szaporodó pluripotens őssejtvonalakat.
A pluripotens embrionális őssejtek korlátlan számú osztódásra képesek, és korlátlan ideig megtartják differenciálatlan állapotukat, ezenkívül – az embrionális őssejteket visszajuttatva az embrióba – képesek bekapcsolódni a normális embrionális fejlődés menetébe. Ugyanakkor már nem képesek az embriót tápláló környező szövetek létrehozására. Az embrionális csíralemezek kialakulása után megkezdődik az embrió sejtjeinek specializálódása: ideg-, izom- és bőrsejtekké stb. alakulnak, mivel ez a feltétele a szövetek, szervek és testformák létrejöttének. Mindezek áraként a sejtek elveszítik „mindenre képes” esélyüket. A magzati fejlődés, de egész életünk során is kis számban megmaradnak viszont olyan nem-specializálódott sejtek, melyeket szöveti őssejteknek nevezünk.
Pluripotens őssejt: Valamennyivel csökkent potenciával rendelkező őssejt, mely nem képes extraembrionális szövet létrehozására, azonban mindhárom csíralemez kialakítására és ivarsejtek képzésére is alkalmas. Ilyen az embrionális vagy az indukált pluripotens őssejt.
Multipotens őssejt: Jelentősen csökkent potenciával rendelkező őssejt, amely nem képes ivarsejtek és egyes szövetek létrehozására, ám több sejttípus is kifejlődhet belőle. Ilyenek a szervezet szöveti őssejtjei.
Unipotens őssejt: egyetlen sejttípust képes előállítani, de képes a megújulásra, ami megkülönbözteti a nem őssejt testi sejtektől (ilyenek például az izomőssejtek).
A születéskor a köldökzsinórból nyert vér is ilyen őssejteket tartalmaz. A szöveti őssejtek a test javítómechanizmusaként szolgálnak, a specializált sejteket frissítik, ugyanakkor a folyamatosan megújuló szervek – mint a vér, a bőr vagy az emésztőrendszer szövetei – normális frissülésében is közreműködnek. Ezek az őssejtek már csak bizonyos szövetek előállítására képesek; minden szöveti őssejt főként az adott szövet sejttípusait állítja elő. Például a csontvelőben megtalálható vérképző őssejtekből kialakulhat az összes vérsejttípus (vörösvérsejtek, fehérvérsejtek és vérlemezkék). A szöveti őssejteket először a csontvelőben találták meg. Ma már mindinkább úgy tűnik, hogy kivétel nélkül minden szövetben jelen vannak, csak még nem mindenhol sikerült őket azonosítani. Ám a felnőtt szöveti őssejtek a szerveinkben igen kis mennyiségben fordulnak elő, ezért begyűjtésük nehéz és összetett feladat.
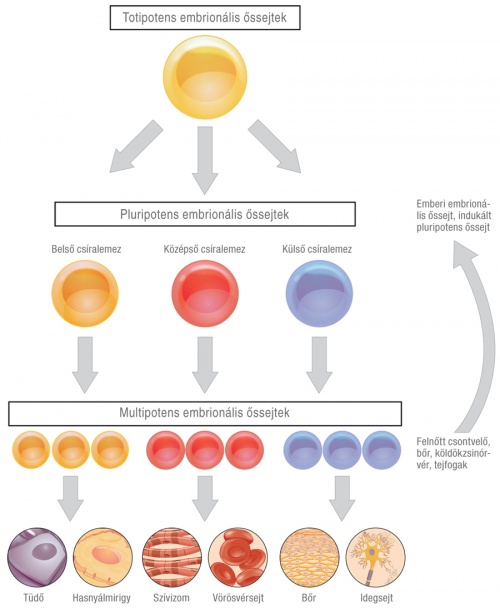 Embrionális őssejtből kialakuló sejtek folyamata
Embrionális őssejtből kialakuló sejtek folyamataAz éretlen sejtből érett sejtté válás folyamatát korábban véglegesnek, visszafordíthatatlannak gondolták. A múlt század ötvenes éveiben, illetve a hatvanas évek elején születtek meg azok az eredmények, amelyek azt mutatták, hogy ez nem egészen így van. A sejtmagátültetés technikáját – békasejtek felhasználásával – Robert Briggs és Thomas J. King fejlesztette ki 1952-ben, ám ők még nem állítottak elő életképes embriókat. A tudomány akkori állása alapján nem volt várható, hogy a bevezetőben említett John B. Gurdon „hibrid” sejtjeiből végül életképes élőlények fejlődjenek ki, már a szövetkezdemények megjelenése is kérdéses volt. A módosított petesejtekből azonban először normális, kopoltyús ebihalak nőttek ki, amelyek a hagyományos módon átalakultak kifejlett, tüdővel lélegző békává, és több évig éltek anélkül, hogy bármilyen rendellenességet mutattak volna. Tehát bebizonyosodott, hogy az érett, testi sejt DNS-e minden olyan információval rendelkezik, amelyre a béka valamennyi sejtjének szüksége van, illetve az is egyértelmű lett, hogy a teljes fejlődési program is újra „lejátszható” ennek az információnak az alapján. Így Gurdon elsőként mutatta ki, hogy a szöveti sejtek specializálódása visszafordítható, és kidolgozta az állatok klónozásának alapjait (ezt a kifejezést előtte csak növények szaporításával kapcsolatban használták). A kísérletek természetesen heves szakmai és etikai vitákat váltottak ki.
Több mint harminc év telt el Gurdon korszakalkotó kísérlete után, mire sikerrel jártak az első emlőssejteken végzett hasonló kísérletek. Elsőként Ian Wilmutnak és munkatársainak sikerült 1996-ban klónozott emlősállatot létrehozniuk úgy, hogy egy felnőtt birka bőrsejtjének magját egy magjától megfosztott birkapetesejtbe ültették át. Az életképes utód, a világhírű Dolly bárány genetikailag azonos volt a bőrsejtet biztosító „donor” állattal. A következő évtizedben több állatfaj esetében sikerült életképes egyedeket létrehozni. Jelenleg huszonkét állatfaj, túlnyomórészt emlős fajok esetében számoltak be sikeres klónozásról – írta a Magyar Tudományban Sarkadi Balázs és Apáti Ágota. A klónozás célja a fejlődésbiológiai kutatásokon kívül a veszélyeztetett állatfajok megóvása (például vadmacska, farkas), illetve állatnemesítés (szarvasmarha, ló, kutya) is lehet, de ugyancsak számos esetben cél volt az emberi gyógyításban felhasználható fehérjék vagy sejtek előállítása. Ugyanakkor persze az emberek félelme is megerősödött a tulajdonképpen lehetséges, de szerencsére mindenhol a világon tiltott emberi klónozás esetleges következményeivel kapcsolatban.
A japán Jamanaka Sinja 2006-ban tette közzé azt a felfedezését, hogy az egér érett szöveti sejtjeit petesejtek jelenléte és felhasználása nélkül, genetikai módszerekkel vissza lehet programozni pluripotens őssejtekké. Jamanaka először egérsejteken, majd egy éven belül emberi sejteken is sikerrel alkalmazott módszerének lényege, hogy néhány speciális gén bejuttatásával az érett bőrsejtekből indukált pluripotens őssejtek (iPS) hozhatók létre. Az eljárás olyan hatékonynak bizonyult, hogy ma már a módszerek egész tárháza áll rendelkezésre iPS-sejtek létrehozására attól függően, hogy a hatékonyság, a biztonság vagy tudományos ismeretek bővítése a cél.
Jamanaka és Gurdon felfedezései alapjaiban változtatták meg a sejtek specializálódásáról alkotott képet. Ma már tudjuk, hogy az érett sejtnek nem kell feltétlenül örökre az elért specializálódott állapotban maradnia. Eredményeik újraírták a tankönyveket, és új kutatási területek nyíltak meg. A szakma egyöntetű véleménye szerint Jamanaka és Gurdon jogosan kapta meg a 2012-es orvosi Nobel-díjat, bár sokan hozzáteszik, hogy Ian Wilmut is korszakalkotó eredményt ért el Dolly bárány létrehozásával.
Az első embrionális őssejtvonalat hólyagcsíra állapotú egérembrióból hozták létre, több mint negyedszázada. Azóta kiderült, hogy az ember korai embrióiból is kinyerhetők pluripotens őssejtek, amelyek tenyészthetők, és belőlük a szervezet minden sejttípusa (kivéve a magzatburok sejtjeit) létrehozható. James Thomson és munkatársai 1998-ban számoltak be arról, hogy sikerült előállítaniuk humán embrionális őssejtvonalakat olyan fel nem használt hólyagcsíra állapotú embriókból, amelyeket az in vitro megtermékenyítést követően nem ültettek vissza, hanem kutatási célokra adományoztak. A humán őssejtvonal létrehozásának módja részben eltér az egér embrionális őssejtjeinek esetében alkalmazottaktól, a tenyésztő médium komponensei sem teljesen azonosak.
Az emberi embrionális őssejtek a mesterséges megtermékenyítési programok során beültetésre nem kerülő embriókból nyerhetők ki. Világszerte számtalan embriót hoznak létre a „lombikbébi programokban”, amelyek egy része mélyhűtéssel évekig tárolható, ám sorsukról végül dönteni kell. A két lehetőség: elpusztításuk, illetve felajánlásuk tudományos kutatási célokra. Pluripotens őssejteket a négy-öt napos embriókból lehet kinyerni: ekkor körülbelül 50-100 sejtből állnak. Az embriócsomókból úgynevezett embrionális őssejtvonalak hozhatók létre, amelyek a többi őssejttel ellentétben korlátlanul osztódnak az in vitro tenyésztés során.
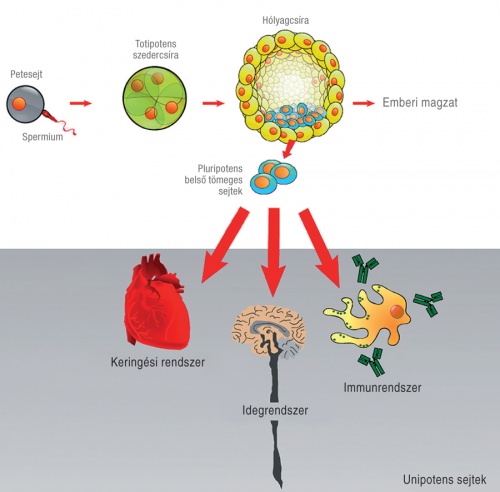 A magzati fejlődés során specializálódó sejtek – szöveti őssejtek kialakulásának folyamata
A magzati fejlődés során specializálódó sejtek – szöveti őssejtek kialakulásának folyamataAz embrionális őssejtek létrehozását és felhasználását számos országban világnézeti, etikai viták kísérik, megosztva a közvéleményt, a kutatókat és a politikai döntéshozókat egyaránt. Ebben a kérdésben nincs egységes álláspont vagy legalább általánosan elfogadott irány. Sarkadi Balázs szerint ahány ország, annyi megoldás. Embrionális őssejteket mindig olyan embriókból állítanak elő, amelyeket elpusztításra szántak. Egyes vallások képviselői az embriókat már élő embernek tekintik, az ilyen sejtekkel való kísérletezés ezért számukra etikailag elfogadhatatlan. Más vallási közösségek sokkal megengedőbbek e tekintetben. Szerencsére ma már embriók elpusztítása nélkül is elő lehet állítani ilyen őssejteket, az indukált pluripotens őssejtek előállítására pedig gyakorlatilag bármilyen szövetünk alkalmas. Jóllehet napjainkban az embrionális őssejtek alkalmazása háttérbe szorult, egyelőre még fontos szerepet játszanak az indukált pluripotens őssejtekkel történő összehasonlítások során.
Az iPS sejtek esetében nem merülnek fel az embrionális őssejtekkel kapcsolatos etikai problémák. Az ilyen őssejtek az emberi fejlődés embrionális szakaszának modellezésére, illetve a sejtterápiás kutatások számára is sejtforrásként szolgálnak. Az orvosi kutatások és a gyógyítás már részben megvalósuló nagy ígérete, hogy beteg emberektől nyert (ős)sejtek segítségével a betegséget hordozó szövetek hozhatók létre, amelyeken célzott gyógyszereket lehet kipróbálni. A szakemberek reményei szerint a betegségekben jelentkező súlyos szövetkárosodások a saját sejtekből létrehozott őssejtekkel, az immunrendszer védekezése nélkül válnak helyreállíthatóvá.
Az őssejtek tehát életbevágó fontosságú egészségmegőrző szerepet tölthetnek be a szervezetünkben. A pluripotens őssejteknek azonban jelenleg, több mint egy évtizednyi kutatás után sincs elfogadott (nem kísérleti) terápiás célú felhasználása. „Nem utolsósorban azért, mert a pluripotens őssejteknek a közvetlen befecskendezésük után valamilyen jelre van szükségük ahhoz, hogy éppen a megfelelő típusú sejtekké differenciálódjanak, és ne például daganatsejtekké” – hangsúlyozza Sarkadi Balázs. A megfelelő irányban differenciálódott sejteket már használhatnánk a gyógyításban, de alapvető biztonsági kérdés, hogy ne daganatot okozó sejtek kerüljenek a beteg szervezetébe. A pluripotens őssejteknél a kezdeteknél tartunk, ugyanakkor a szöveti eredetű őssejteket már negyven éve alkalmazzák gyógyításra, például a csontvelő-átültetés során. Szöveti őssejtekből napjainkban csontot, porcot, akár szövetpótló anyagokat is készítenek, egyre több irányban indul meg az alkalmazásuk.
Sarkadi Balázs a legígéretesebb irányok egyikeként a szöveti őssejtek immunológiai és szövethelyreállító felhasználását tartja. A kötőszövetből, de akár a zsírszövetből is kivonható, úgynevezett mezenchimális őssejtek immunszupresszívek, azaz gátolják az immunválaszt. E tulajdonságuknak köszönhetően súlyos immunológiai betegségek esetén használhatók, és ma már gyógyító készítményként is elérhetők. A vérképzőrendszer helyreállítása szinte már rutin klinikai eljárássá vált. A csontvelőből vagy a köldökzsinórvérből kinyert szöveti őssejtek alkalmazása ugyanakkor egyre inkább elterjed, ezeket például érelzáródások megszüntetésénél is sikeresen kezdik használni. A szemben a szaruhártya vagy az ideghártya újraképzésénél is lehetséges a felhasználásuk. Ma elfogadott, hogy olyan betegségeknél, ahol speciális szövetek előállítása megoldást jelenthet, főleg szöveti őssejteket alkalmazhat az orvoslás.
A csontvelő-átültetéskor használt csontvelői őssejtekből viszonylag sok van a szervezetünkben. A köldökzsinórvérben az előbbihez hasonló (elsősorban vérképző) őssejtek találhatók. Ebből a két forrásból viszonylag sok szöveti eredetű őssejtet lehet kinyerni, illetve a zsírszövetben és az izomszövetben, de még a foggyökérben is találni olyan őssejteket, amelyekből az adott szövetek újraképződnek. Ahol nagyon kevés őssejtünk van, az a szív és az idegrendszer, ezek a szervek csak nagyon korlátozott mennyiségben tudnak újraképződni. „Valószínűleg azért, mert semmi jóra nem vezetne, ha ezek a nagyon gondosan megszervezett szövetek nagyon gyorsan átalakulnának. Ezeknél nem jó irány az újratervezés” – véli Sarkadi Balázs. Ugyanakkor a legsúlyosabb emberi betegségek éppen ezeket a szerveinket érintik, így érthető a kutatók fokozott igyekezete az őssejtek ilyen irányú felhasználására.
A pluripotens őssejteket napjainkban egyelőre mégis inkább a kutatásban tartják ígéretes lehetőségnek. Ott is elsősorban a személyre szabott gyógyszertervezésben. A betegből nyert szöveti őssejtekből vagy a létrehozott iPS sejtekből a kutatók különböző betegségmodelleket hoznak létre. A beteg őssejtjének segítségével így például emberi szívizmot, idegsejteket lehet létrehozni, majd azokon gyógyszermolekulákat lehet kipróbálni, vizsgálni azok hatékonyságát vagy éppen toxicitását. Az ilyen, pluripotens őssejtekkel folyó kutatás részben alapkutatás jellegű, de gyakran gyógyszerfejlesztési célokra irányul. A terápiás alkalmazás még a kezdeteknél tart. Az igaz, hogy az iPS sejtek könnyen előállíthatók és korlátlan ideig fenntarthatók, de a tenyésztés maga még nagyon drága – a reagenseket aranyárban mérik –, ezért e kutatási terület művelését óriási pénzekkel támogatják szerte a világon. Így azután laboratóriumok és intézetek százai alakultak ilyen kutatásokra, és óriási a verseny az eredményekért.
Az ígéretes kutatások körében mindenképpen szólnunk kell a komplex háromdimenziós sejtrendszerekről. Efféle rendszereket már emberi sejtekből is megpróbálnak létrehozni: ilyen például a tenyésztőedényben kialakítható „miniagy” megalkotása. Az előre kialakított „állványzatra” növesztik rá adott típusú idegsejtek hálózatát, így azok kialakíthatják különleges kapcsolataikat és hálózataikat is. A kutatók azt remélik, hogy ily módon megtanulható, miként kommunikálnak egymással az idegsejtek. Ennek megértése a legkülönbözőbb neurológiai és a pszichiátriai betegségek kezeléséhez vihet közelebb, hiszen az elromlott szerkezeteket közvetlenül vizsgálhatják.
Kinek az érdeke az ilyen irányú kutatások finanszírozása? Sarkadi Balázs szerint mindazoknak, akik érdekeltek abban, hogy jobban megismerjük az emberi szervezet felépítését, többet tudjunk a sejtek és a szövetek működéséről, jobban megértsük a daganatok kifejlődését. A gyógyszerek kipróbálásának útja is mindinkább az emberi sejteken, szöveteken való tesztelés. És végül egyértelműen elmondható, hogy az őssejtekkel kikísérletezett eljárások előbb-utóbb terápiásan is alkalmazhatóak lesznek a súlyos emberi betegségek gyógyításában.
Az akadémikus szerint nagyon sok párhuzamosság van a humán és az állati őssejtekkel folyó kutatásokban, de nem minden eredmény összevethető, megfeleltethető. Az egér embrionális őssejtjei például hajlandóak a nagyon gyors osztódásra, akár már egyetlen sejtből is kitenyészthető egy egész kolónia. Az emberi sejtek erre egyesével nem igazán hajlandóak, kisebb telepekben érzik jól magukat, csak így képesek osztódni. Sarkadi Balázs szerint a sok ígéretes kísérleti adat ellenére sincs még olyan technológia, amivel a humán pluripotens őssejtek társas igényét egyértelműen megkerülhetnénk. Ugyancsak különbség, hogy más anyagokra érzékenyek, másként növekszenek a humán és az állati embrionális őssejtek. Ezért gyakran nem lehet „lefordítani” az állati őssejteken tanultakat az emberi őssejtekre.
Ahogy a tudomány minden más területén, az őssejtkutatók körében is hatalmas az eredménykényszer. Óriási a verseny, több ezer laboratórium dolgozik a világban. A versenyzés kényszere olykor tévútra viszi a kutatókat.
A kobei Riken Biológiai Fejlesztések Központjának kutatói tavaly januárban jelentették be, hogy egy vadonatúj eljárást fedeztek föl, amivel pluripotens őssejtté alakíthatók a felnőtt szöveti sejtek. A kutatók néhány hónappal később elismerték, hogy a Nature-ben megjelent tanulmányukban számos tévedés van, mivel meghamisított adatokra épül. A tanulmány vezető szerzője, Obutaka Haruko nemcsak a publikációban szereplő képeket manipulálta, de az általa leírt sejtvonaltípus valószínűleg nem is létezik, mivel azóta senkinek sem sikerült a sejtvonalakat létrehoznia. Szomorú vége a történetek, hogy a laboratórium szakmai vezetője elkeseredésében – a japán hagyományok nyomán – öngyilkosságot követett el.
Sarkadi Balázs szerint az, hogy valahol valakik manipulálnak, nem a tudományág sajátossága, hanem csak azt mutatja, hogy csalók, etikátlan emberek mindenütt vannak. „Ahol nagy a verseny, ahol nagyon sokan dolgoznak ugyanazon a területen, ott felerősödhetnek a nem kívánatos jelenségek. A tudomány egyik feladata és alapvető sajátossága éppen az, hogy kiderülnek a turpisságok. Ha egy kísérlet nem reprodukálható, nehezen magyarázható, annak kitalálója belebukik” – jegyzi meg Sarkadi Balázs.
Mezőgazdasági szempontból az állati embrionális őssejtek értékes génsebészeti eszközök lehetnek az állatállomány előnyös génekkel való javításához. Erről tavaly a Természet Világa című lapban írt Németh Kinga és Gócza Elen. Ennek egyrészt gazdasági jelentősége van, másrészt a betegségekkel szembeni ellenállás szempontjából is fontos. Nagy szerepe lehet a génmegőrzés területén, továbbá az embrionális őssejtek jól használhatók az emlősök funkcionális genomikai kutatásaihoz is. Orvos-biológiai szempontból is nagy jelenősége van a megfelelő állati őssejtvonalak alapításának, hiszen ezek segítségével hatékonyan hozhatók létre olyan modellállatok, melyek segítségünkre lehetnek egyes humán betegségek vizsgálatában, illetve ezek kezelésében és gyógyításában.
Az egérrel szemben a patásokból származó embrionális őssejtvonalak sejtjei lassan osztódnak, gyorsan szövetekké differenciálódnak a tenyésztés során. A patások embriócsomójában található sejtek pluripotensek, mivel képesek az új utód szöveteinek létrehozására, de jelenleg még nem lehet tudni, hogy az embrionális fejlődés során melyik az az optimális időpont, amikor az egér embriócsomójában található sejtekhez hasonló, valóban pluripotens sejteket lehet izolálni. Ez a probléma nem egyedül a patásoknál létezik, mivel a sejtvonal-alapítás sikeressége rágcsálók esetében is függ a genetikai háttértől. Haszonállatoknál az embrionális őssejtvonalak esetében rengeteg még a tisztázandó kérdés. Biztató jelnek tekinthető azonban az, hogy az elmúlt években a gazdasági haszonállatok esetében is sikerült iPS sejtvonalakat létrehozni.
A gazdasági haszonállatokkal folyó őssejtkísérletek jelentőségét Gócza Elen abban látja, hogy ezekkel olyan modellállatokat lehetne létrehozni, amelyek segítségével az eddig alkalmazott transzgenikus egereknél jobban lehetne modellezni számos humán betegséget. Sertés pluripotens őssejtek olyan transzgenikus sertések előállítását tennék lehetővé, amelyek szerveit később esetleg xenotranszplantáció – azaz nem emberi eredetű sejtek, szövetek, szervek átültetése emberbe – során használhatnák. A gödöllői Nemzeti Agrárkutatási és Innovációs Központ Mezőgazdasági Biotechnológiai Kutatóintézetének tudományos tanácsadója azt is elmondta magazinunknak, hogy a sertés, a szarvasmarha, illetve a nyúl pluripotens őssejttenyészetekből jelenleg nem lehet ivarsejt kiméra (kiméra: amikor egy egyed szervezetében két vagy több embrióból vagy szövetből származó, eltérő genotípusú sejt található – a szerk.) állatokat létrehozni, emiatt ennek hiányában célzott genetikai módosításokat hordozó modellállatokat sem. Ennek valószínűleg az az oka, hogy ezek a sejtvonalak nem a korai, az egér embriócsomójában található sejteknek megfelelő, úgynevezett naiv állapotban levő sejtekből származnak, hanem egy olyan, már differenciáltabb sejttípusból, amelyből ivarsejtek nem tudnak kialakulni.
Gócza Elen a növényi őssejtekkel a világban folyó kutatásokkal kapcsolatban elmondta, hogy a növényi őssejtek alkalmazásának nagy jelentősége van a növényi regenerációs és fejlődésbiológiai vizsgálatokban. Emellett a növényi őssejtkivonatok értékes forrásai számos hatóanyagnak. A növényi őssejtek nagy mennyiségű hatóanyag előállítására alkalmasak, amelyek felhasználásával például olyan kozmetikumok hozhatók létre, melyek alkalmasak a bőr rugalmasságának, hidratáltságának megőrzésére.•























