Molekuláris Lego: fragmens építőkészletek a gyógyszerkutatásban
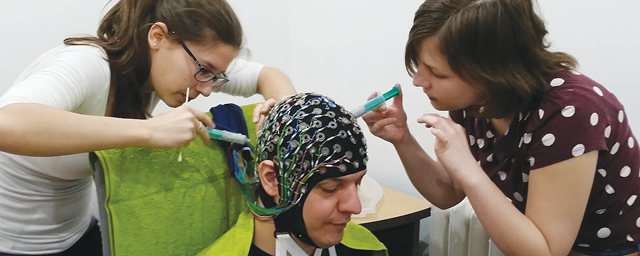
 A kutatócsoport tagjai (balról jobbra): Kelemen Ádám, Csányi Dorottya, Kiss Dóra Judit, Visy Julianna, Balog József András, Hont Péter, Takács Daniella, Bajusz Dávid, Szilágyi Bence, Ábrányi-Balogh Péter, Hegedűs Lászlóné, Csimbók Ervin, Ferenczy György, Kovács Péter, Kónya Dénes, Keserű György Miklós.
A kutatócsoport tagjai (balról jobbra): Kelemen Ádám, Csányi Dorottya, Kiss Dóra Judit, Visy Julianna, Balog József András, Hont Péter, Takács Daniella, Bajusz Dávid, Szilágyi Bence, Ábrányi-Balogh Péter, Hegedűs Lászlóné, Csimbók Ervin, Ferenczy György, Kovács Péter, Kónya Dénes, Keserű György Miklós.A kutatócsoportban – a Nemzeti Agykutatási Program (NAP) tematikájának megfelelően – a központi idegrendszer megbetegedéseinek kezelésére alkalmas új vegyületek azonosításán dolgoznak. A NAP hálózatán belül a Richter Gedeon Nyrt. mellett gyorsan fejlődő együttműködések alakultak ki az MTA KOKI és a Semmelweis Egyetem egyes kutatócsoportjaival. A kutatócsoport a gyógyszerkémia területén folytat önálló kutatási programokat és nyújt technológiai platformot a NAP más kutatócsoportjai számára. Az új technológiai megoldások közül kiemelkedő a Magyarországon elsőként bevezetett fragmens alapú gyógyszerkutatási platform, amelynek lényege a molekuláris Lego megközelítés.
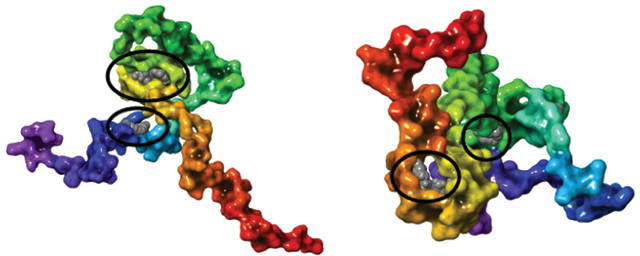
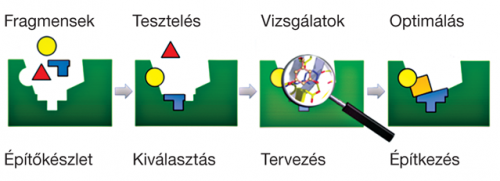
Már több mint száz esztendeje annak, hogy Emil Fischer és Paul Erlich a gyógyszerek hatékonyságát a molekulák és a szervezet fehérjéi között kialakuló molekuláris kölcsönhatásokra vezette vissza. A fehérjék szerkezetéről szerzett ismeretek bővülésével az is kiderült, hogy a gyógyszermolekulák hatásukat azáltal fejtik ki, hogy a fehérjék kisebb-nagyobb üregeibe kötődnek. Az ilyen üregek, valamint a bennük megfelelő kölcsönhatásokat kialakítani képes molekulák azonosítása a gyógyszerkutatás kezdeti szakaszának egyik legnagyobb kihívása. A múlt század végéig az üregekbe illeszkedő molekulákat a korábban más célra előállított molekulák közül próbálgatással igyekeztek kiválasztani. Az utóbbi tíz évben, egy új megközelítésnek köszönhetően, a gyógyszereknél lényegesen kisebb méretű molekulák (fragmensek) tesztelésén és továbbépítésén alapuló molekuláris Lego módszer alapjait sikerült lerakni. A módszer szerint a ligandumok keresése a fragmensek kötődésének vizsgálatával indul, és azon a felismerésen alapul, hogy az ilyen molekulák nagyobb valószínűséggel kötődnek a fehérjék üregeihez, mint a nagyobb, gyógyszerjelölt méretű molekulák. Ennek következménye, hogy már néhány száz vagy néhány ezer fragmenst tartalmazó könyvtár szűrővizsgálata is kiindulópontul szolgáló találatot adhat. A kiindulópontoknak az üreg jellegzetességeit figyelembe vevő továbbépítése, vagy több találat esetén összekapcsolása új gyógyszerjelöltekhez vezethet (ábra).
A kutatók által az elmúlt években elért eredmények nemzetközi érdeklődést keltettek, több alkalommal közölte ezeket a terület vezető folyóirata, a Nature Reviews Drug Discovery is. A NAP-támogatás arra is lehetőséget teremtett, hogy a kutatócsoport tökéletesíthesse az eddig általánosan használt építőelemek gyűjteményét, és egy koncepcionálisan új fragmens könyvtárat hozzon létre. Az új koncepció alapja, hogy a fehérjék kötőhelyén kialakuló kölcsönhatások véges számú mintázatot adhatnak, így a lehetséges mintázatok számítógépes modellezésével kiválasztható az építőelemeknek egy olyan készlete, amely maximális számú kiindulópontot szolgáltat. A megközelítésre és ennek sikeres megvalósítására figyelt fel az amerikai BioBlocks, velük az új fragmens könyvtár továbbfejlesztésére és hasznosítására kötöttek együttműködési megállapodást. A NAP támogatásával a gyógyszeriparból az akadémiai kutatásba integrálódó kutatók nemcsak a kutatási tematika megújításában vehettek részt sikerrel, de eredményeik már rövid távon hasznosulhatnak a gyógyszerkutatás nemzetközi gyakorlatában.
A kutatócsoport fragmenseken alapuló megközelítésének továbbfejlesztését szolgálja egy 2016-ban indult konzorciális H2020 MSCA projekt, a FRAGNET is, amelyet az Európai Unió 3,9 millió euróval támogat. A holland, spanyol, svéd, svájci és egyesült királyságbeli kutatócsoportok és vállalkozások által alkotott konzorcium tagjai egy PhD-hallgatókat foglalkoztató Marie Curie képzési hálózatot hoztak létre. A pályázati támogatás tovább erősíti a magyar kutatócsoport törekvését, hogy a fragmens alapú megközelítést kiterjessze kovalens kötésű gyógyszerjelölt molekulák kifejlesztésére. Ezek a molekulák a hatásért felelős fehérjével olyan erős és tartós kölcsönhatást alakítanak ki, amely megakadályozza a gyógyszermolekula távozását a kötőhelyről. A kutatócsoportban ezért kémiailag reaktív fragmenseket tartalmazó építőkészletet terveznek és állítanak elő, továbbá olyan tesztelési eljárásokat fejlesztenek, amellyel az ilyen fragmensek fehérjekötődése vizsgálható. A találatok gyógyszerjelöltekké optimálását részben saját fejlesztésű gyógyszertervező módszerek támogatásával, a fehérjéhez kötött fragmensből kiindulva, annak továbbépítésével végzik. A kifejlesztett molekuláris építőkészletek használatával a magyar kutatók Iwan de Esch (Vrije Universiteit Amsterdam) és Rod Hubbard (University of York) kutatócsoportjaival közösen kívánnak új, innovatív vezérmolekulákat kifejleszteni több, terápiás szempontból fontos fehérje ellen. A megközelítés újdonságát az is mutatja, hogy a konzorcium partnerei között vannak a legnagyobb európai gyógyszergyárak, így a GlaxoSmithKline, a Novartis, a Roche és a Servier is.•
2017. február