Öregedési folyamatok vizsgálata a nagy mocsári csigában
A kutatócsoport modellállata a nagy mocsári csiga (Lymnaea stagnalis). A 94 éves BLKI-ban már több mint 30 esztendeje használják a puhatestű (csiga, kagyló) modellszervezeteket alap- és alkalmazott neurobiológiai és környezettoxikológiai komplex kutatásokhoz. A hazai és nemzetközi tekintetben is elismert kutatócsoport – a NAP 1.0 támogatásával kiépített infrastruktúrát kiaknázva – jelentős eredményeket ért el a NAP 2.0 támogatása révén. Eredményeiket 22 nemzetközileg kiemelten rangos SCI- (Science Citation Index – a szerk.) publikációban (pl. Current Biology, eLIFE, Scientific Reports, Journal of Gerontology), egy könyvfejezetben és számos előadásban foglalták össze.
 Csoportmunka az intézetben
Csoportmunka az intézetbenMinden jó, ha a vége jó
A NAP 1.0 támogatása után örömmel fogtunk bele a NAP 2.0 által támogatott kutatásokba. Az alapvető koncepciónk nem változott: a Balatonból kimutatható emberi eredetű gyógyszermaradványok (pl. fogamzásgátlók, pszichoaktív hatóanyagok) gerinctelen vízi modellszervezetekre gyakorolt idegélettani hatásaival kívántunk foglalkozni. A kutatócsoport mind létszámában, mind szaktudásában megfelelt a tervezett kutatásoknak, továbbá nemzetközi és hazai kollaborációk területén is jól álltunk. Például 2019 szeptemberétől három hónapot töltött nálunk Vértes Ákos (The George Washington University, USA) egy MTA vendégprofesszori támogatás keretében, amikor az egy-sejt mintavételezést, illetve az 1-3 pL minta metabolomikai és peptidomikai elemzését dolgoztuk ki a nagy mocsári csiga központi idegrendszerének azonosított idegsejtjeiben (Frontiers in Molecular Neuroscience).
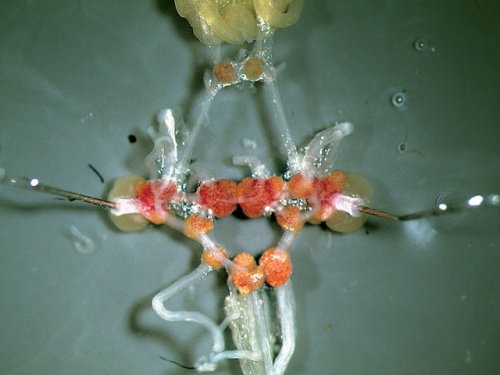 A nagy mocsári csiga központi idegrendszere
A nagy mocsári csiga központi idegrendszereAmivel nem számolhattunk a második támogatási periódus kezdetén, az a koronavírus-pandémia, illetve intézetünk szervezeti átalakítása, annak leválasztása az Ökológiai Kutatóközpontról (ÖK), ami jelentős mértékű kapacitást vont el a tervezett kutatásoktól. Aztán 2021 elején ismét jól alakultak a dolgok, hiszen az Eötvös Loránd Kutatási Hálózat (ELKH) 2020. novemberi döntésének értelmében ténylegesen megtörtént a BLKI ÖK-ból való kiválása, az új igazgató, Erős Tibor pedig támogatólag állt a NAP 2.0 pályázat minél sikeresebb megvalósításához. E nyugodtabb időszakban az MTA Bolyai János kutatási ösztöndíja mellett egy nemzetközi kooperációban megvalósuló OTKA-pályázatot is elnyertünk. A kutatócsoport egyik elhivatott, Kooperatív Doktori Program hallgatói ösztöndíjas doktorandusza, Fodor István 2021-ben a Veszprémi Akadémiai Bizottság Kiemelkedő Ifjú Kutatója elismerésben részesült.
Több van a nagy mocsári csiga kutatásában, mint azt korábban gondoltuk
 A nagy mocsári csiga
A nagy mocsári csigaKutatócsoportunk, részben a NAP 2.0 támogatásával, együttműködésben a Pécsi Tudományegyetem Általános Orvostudományi Karának (PTE ÁOK) több intézetével, 137 emberi eredetű hatóanyagot monitorozott a Balatonban és annak vízgyűjtő területén. Ezek közül 74-et mutattunk ki a vízrendszerben, leírtuk azok tér- és időbeli eloszlását és koncentrációviszonyait. Megbecsültük az egyes hatóanyagok ökológiai kockázatát, ökotoxikológiai adatok és a környezeti koncentrációik ismeretében. Jellemeztük a vizsgált hatóanyagok egyed-, sejt- és molekuláris szintű komplex hatásait a csigában, multidiszciplináris megközelítést alkalmazva.
A 74 hatóanyag közül a legmagasabb koncentrációban (~1 µg/l) és a leggyakoribb előfordulással (>95%) az antiepileptikumok (pl. karbamazepin, lamotrigin), az opioid fájdalomcsillapítók (pl. tramadol) és az antidepresszánsok (pl. triapride) mutathatók ki. Jelenleg vizsgáljuk az antiepileptikumok hatását, hiszen ismeretes, hogy hatóanyagaik gyakran a glutamát serkentő neurotranszmitter felszabadulását gátolják. Ez a transzmitter sok egyéb mellett fontos szerepet játszik a tanulási és memóriafolyamatokban, ezzel összefüggésben pedig az időskori memóriavesztésben is érintett lehet. Vagyis azt várhatjuk, hogy ha az olyan hatóanyagok, mint például a lamotrigin, hatnak a vízben élő állatok, például csigák központi idegrendszerére, akkor azokban gátlódik a glutamátfelszabadulás, aminek következtében az NMDA-receptor-aktivitás gátlásán keresztül sérülhet a hosszú távú memória (LTM) kialakulása, és az eltárolt emléknyomok felidézésének lehetősége is.
Az öregedéssel járó folyamatok gerincesekben történő vizsgálata – idegrendszerük komplexitása miatt – nem egyszerű feladat a hálózatok és az egyedileg azonosított idegsejtek szintjén. Ennek következtében az öregedéskutatás nagymértékben támaszkodik például a nagy mocsári csigára, amely évtizedek óta jól ismert és kedvelt modellszervezete az öregedés- és memóriakutatásnak is. Csoportunk az angliai Sussex Egyetem School of Life Sciences (Kemenes György, Kemenes Ildikó) és a PTE ÁOK Anatómiai Intézet (Reglődi Dóra) kutatóival együttműködve már vizsgálta, hogy milyen hatással van a PACAP-fehérje és az IGF-1 hormon az öregedéssel járó, idegrendszerben lejátszódó folyamatok visszafordítására. Megállapítottuk, hogy nagyon is lehetséges a neurális hálózatokat farmakológiailag „újraprogramozni”, és az idős állatokat „megfiatalítani” a memória javítása érdekében. A szóban forgó folyamatok részletes molekuláris hátterét az evolúciósan konzervált, releváns kulcsmolekulák szekvenciáinak hiányában ez idáig nem lehetett vizsgálni. Azonban a Joris Koene által vezetett holland kutatócsoporttal (Vrije University, Amszterdam) részt vettünk a nagy mocsári csiga genomjának azonosításában, és a munka során olyan gerinces homológ géneket azonosítottunk (pl. klotho, PARK7/DJ1, α-secretase stb.), amelyek az emberi öregedésében, vagy olyan humán eredetű neurodegeneratív betegségek, mint például a Parkinson- vagy az Alzheimer-kór kialakításában is kulcsszerepet játszanak (The Journal of Gerontology).
A „Lymnaea öregedési modell” használatával jelenlegi célunk a tanulási folyamatokban feltehetően kulcsszerepet játszó, konzervált gének manipulálásával lassítani az öregedés során kialakuló memóriacsökkenést.•


























