Mi olvasható ki a mutációs mintázatokból?
A Budapesti Fazekas Mihály Gyakorló Általános Iskola és Gimnáziumban tett érettségi után a Trinity College-ban (Cambridge) biokémiát tanult Szüts Dávid, majd ugyanitt PhD-fokozatot szerzett. A cambridge-i évek után Londonban vezetett kutatócsoportot, ahonnan az MTA Lendület pályázatának nyerteseként 2011-ben tért haza. A Cambridge-ben elkezdett témát hozta haza, s alapított a kidolgozásra önálló egységet. Az öt évre szóló „lendületes” támogatás letelte után a TTK kutatócsoportjaként folytatja a mutációk kialakulásának elemzését. „A DNS mutációja során megváltozik annak kémiai szerkezete, például rácsatlakozik egy oda nem illő molekula. A sejt ezt a hibát kijavítja, visszaalakul a normál DNS, csak éppen az utóbbi szerkezete – ha nem az eredeti bázist teszi a betolakodó molekula helyére – eltér a kiindulási állapottól. Ez a folyamat végbemehet spontán módon, de környezeti tényezők is indukálhatják” – tájékoztatott Szüts Dávid.
Ez azért érdekes, mert a mutáció és a szelekció viszi előre az evolúciót. A mutáció számlájára kevésbé hasznos dolog, a daganatok kialakulása is írható. A daganatos sejtek abban különböznek a normál testi sejtektől, hogy a génállományukban változások, azaz mutációk mentek végbe. A tumorsejtek általános tulajdonságának tűnik a genom instabilitása. Valószínűleg éppen az instabilitás miatt tud kialakulni a daganat. A TTK tudományos főmunkatársa a mechanizmus irányából közelített ehhez a jelenséghez, azaz hogy milyen folyamatok másolják, replikálják a DNS-t. Eleinte lassan haladtak, ám új módszerek jelentek meg a változások detektálására. A hatékonyabb kutatást a nagyjából tíz éve elérhető új generációs DNS-szekvenálás – a genetikai állományt felépítő nukleotid bázisok sorrendjének egyre gyorsabb meghatározása – tette lehetővé. Az első humán genom hárommilliárd bázisát tizenöt év alatt határozták meg több milliárd dollárért. Ma néhány nap alatt pár száz dollárért elkészül egy ember genomja.
Kísérleteik során a kutatócsoport tagjai sejttenyészetes modellben vizsgálták a mutáció folyamatát. Egyetlen sejt génállományát meghatározták, majd utódainak is feltérképezték az összetételét. A két adathalmaz közötti különbség a mutáció. Az elmúlt időszak alapvető jelentőségű munkája volt annak meghatározása, hogy egyes anyagok mennyire generálnak génhibákat. Erről szóló, komoly visszhangot kiváltó tanulmányukban a gyakorta használt kemoterápiás vegyületekkel kapcsolatos tapasztalataikról számoltak be. A kutatók azt találták, hogy lényeges eltérés van a különböző hatóanyagok hatásai között. Ezeknek a tulajdonságoknak az ismerete két szempontból is használható. A beteg egészséges sejtjeit kevésbé károsító hatóanyagot választhat a kezelőorvos, és hogy a tumorsejtben se okozzunk felesleges mutációt, mert ha túl sokat generálunk, akkor tovább változik a daganat, gyorsul a rák evolúciója. (Utóbbi azért káros, mert a folyamat általában a kemoterápiára való rezisztencia megjelenését jelenti. Azaz, maga a kezelés segítheti elő a kezelés romló hatékonyságát.) Szüts Dávid szerint a legtöbb esetben a normális sejtek károsodása nem végzetes, mert ezeknek – a daganatos sejteknél – jobb a DNS-javító képességük.
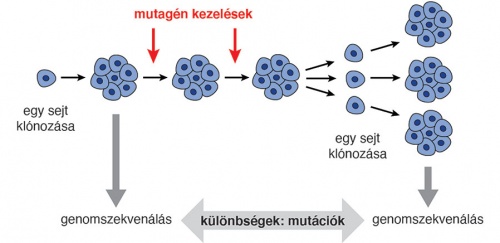 A mutációk detektálásának sémája sejttenyészetben
A mutációk detektálásának sémája sejttenyészetbenA csoport munkájának meghatározó eleme a DNS-javító folyamatok vizsgálata. Olyan sejtekkel dolgoztak, amelyek nem képesek valamilyen javító feladat elvégzésére. A sejtekben ugyanis több javító mechanizmus működik, amelyek külön-külön aktiválhatók. Kiderült, ha valami miatt a javító folyamat egyike leáll, sok mutáció jön létre. Két éve tették közzé azt az eredményt, hogy a homológ rekombináció nevű útvonal inaktiválásával a spontán mutagenezis nyolcszorosára emelkedik. Ugyanezen gének (BRCA1, BRCA2) örökletes hibái nagymértékben hajlamosítanak a daganatok kialakulására. Éppen azért, mert ha bizonyos testi sejtek nagyon sok mutációt termelnek, nagyobb eséllyel rontanak el olyan gént, amely kóros elváltozáshoz vezet.
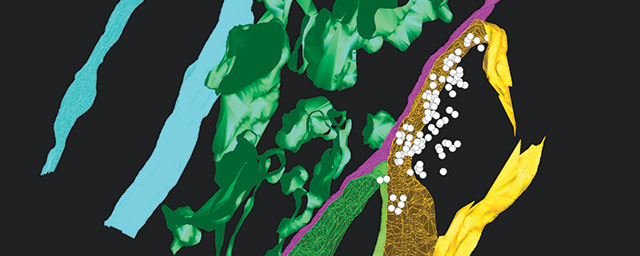
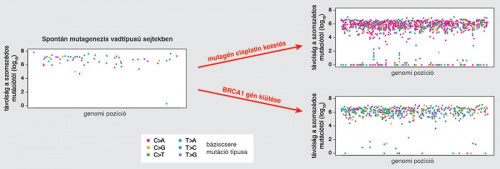 A mutációk kialakulását befolyásolják a környezeti hatások és a DNS-hibajavítás. Vadtípusú sejtekben kevés spontán mutáció alakul ki (bal oldalon, minden pont egy báziscsere). Mutagenikus cisplatin kezelés hatására elsősorban a C->A báziscserék dúsulnak fel, míg a BRCA1 DNS-javító gén kiütésének hatására minden mutációtípus gyakrabban fordul elő.
A mutációk kialakulását befolyásolják a környezeti hatások és a DNS-hibajavítás. Vadtípusú sejtekben kevés spontán mutáció alakul ki (bal oldalon, minden pont egy báziscsere). Mutagenikus cisplatin kezelés hatására elsősorban a C->A báziscserék dúsulnak fel, míg a BRCA1 DNS-javító gén kiütésének hatására minden mutációtípus gyakrabban fordul elő.Ez az eredmény nem marad laboratóriumi keretek között. A betegek kezelésében ugyanis kihasználhatják a tumorsejtek DNS-javításában tapasztalt hiányosságokat – ehhez persze előzetesen tudni kell, hogy mely folyamatok nem működnek. Ha tudjuk, olyan típusú kezelés adható, amelyre az ilyen sejt érzékeny. A BRCA1 és BRCA2 tumor szuppresszor gének hibája például tipikus mutációs mintázatot okoz – az ilyen hibát hordozó sejtek hihetetlenül érzékenyek a PARP nevű enzim gátlószereire. Ezeket a hatóanyagokat öt éve klinikákon használják, és meglepően jó hatékonysággal működnek bizonyos petefészek- és emlődaganatok kezelése során.
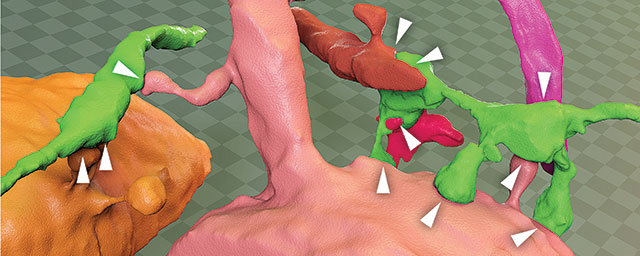
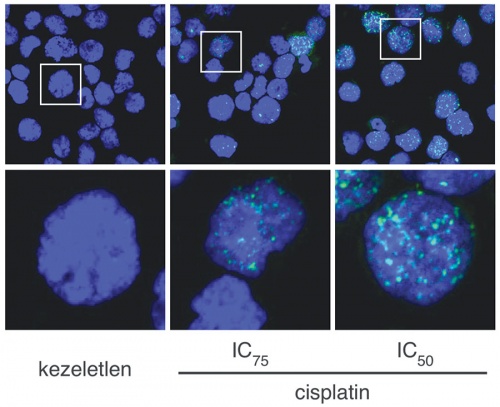 A platinakezelés DNS-károsító hatása. Humán sejtek egyórás cisplatin kezelést kaptak kétféle koncentrációban (IC75: 75% túlélés, IC50: 50% túlélés). A DNS-károsodást, elsősorban DNS-töréseket, a H2AX hiszton fehérje foszforilációja jelzi (zöld szín) a sejtmagokban (DNS, kék).
A platinakezelés DNS-károsító hatása. Humán sejtek egyórás cisplatin kezelést kaptak kétféle koncentrációban (IC75: 75% túlélés, IC50: 50% túlélés). A DNS-károsodást, elsősorban DNS-töréseket, a H2AX hiszton fehérje foszforilációja jelzi (zöld szín) a sejtmagokban (DNS, kék).Hogy megtudjuk, bizonyos ráknak melyik DNS-javító mechanizmusa romlott el, meghatározzák azon gének szekvenciáját, amelyek el szoktak romlani. Ez a módszer azonban nem hatékony, mert a meghatározás bonyolult, ráadásul előfordulhat, hogy más gének működése ment tévútra – miközben a sejtben azonos problémát okoz. „Mi nem a gén, hanem a kiváltott hatás felől közelítünk a feladathoz. A genom teljes meghatározása után nem konkrét génhibákat, hanem mintázatokat keresünk. Nem az érdekel minket, hogy melyik gén romlott el, hanem az, hogy melyik folyamat nem működik” – magyarázta Szüts Dávid, aki szerint a továbblépésnek két útja képzelhető el. A sejtek működéséhez érdeklődő tudósként közelítő kutató a mechanizmus minél alaposabb feltárására koncentrál a jövőben. Annak a kiderítése is izgalmas, hogy milyen mechanizmusok őrzik az eredeti génállományt a normálisan működő sejtekben. Klasszikus alapkutatásról van szó, ahol élősejtek mellett in vitro kísérleteket is végeznek. Hasonlóan izgalmas lehetőség új, támadható célpontok feltérképezése a daganatos sejtekben. Ezen a téren enzimgátló szerek és speciális DNS-sérüléseket okozó hatóanyagok egyaránt szóba jöhetnek.•