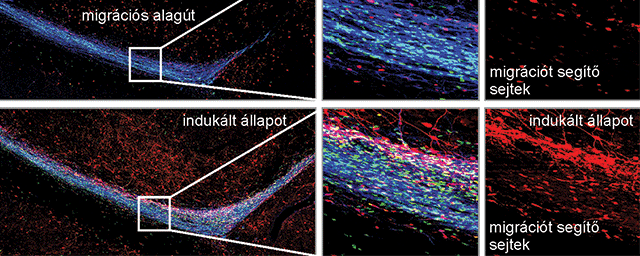
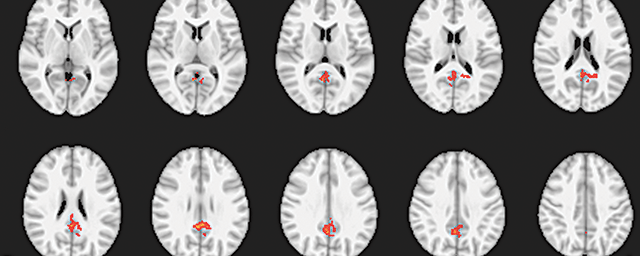
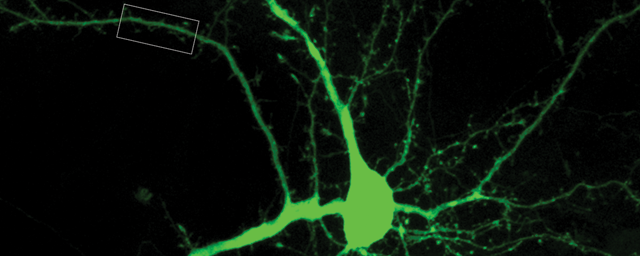
Neuropatológiai vizsgálatok a NAP keretében
Bencze János PhD-hallgatót arról kérdeztük, hogy fiatal kutatóorvosként mit nyújtott számára a Nemzeti Agykutatási Program, a NAP?
– Abban a szerencsés helyzetben vagyok, hogy 2013 szeptembere, tehát a NAP indulása óta részese lehetek a Hortobágyi Tibor által vezetett neuropatológiai kutatócsoportnak. Kezdetben még tudományos diákkörösként, több mint egy éve pedig PhD-hallgatóként „élvezhetem” a Nemzeti Agykutatási Program előnyeit. Elsőként agytumorok (meningeomák) kutatásával foglalkoztam Csonka Tamás és Murnyák Balázs (korábbi PhD-hallgatók) segítségével. Sikerült egy több fehérjét vizsgáló immunhisztokémiai panelt létrehoznunk, amely a klinikai progresszió becslésében használható. Az itt elért eredményeket hasznosítva kezdtem meg a sejtciklust szabályozó fehérjék neurodegenerációban betöltött szerepének tanulmányozását. Azonban meg kell jegyezni, hogy minden tudományos tevékenység egyfajta vállalkozás, ahol a siker záloga a működéshez szükséges minimális feltételek megteremtése. Ugyanakkor a NAP nemcsak financiális szempontból jelentős, hanem mára komoly eszmei értéket is képvisel mind a magyar, mind a nemzetközi tudományos életben. Örülök, hogy már orvostanhallgató korom óta részese lehetek a programnak.
 Bencze János
Bencze JánosMik a tervei a jövőre nézve, milyen hatással lesz az Ön által végzett munkára a NAP első szakaszának lezárása?
– Részese lehetek a második „felvonásnak”, így az eddigi munka tovább folytatódhat. Úgy érzem, jó úton járok, és hosszabb távon is az idegrendszer kutatásával szeretnék foglalkozni. Jelenleg időm nagy részét a neurodegeneratív demenciák tanulmányozása tölti ki. Ezt olyan érdekes és ígéretes területnek tartom, amelynek komoly hatása van nemcsak az orvostudományra, hanem a szociális ellátórendszerre és az egész társadalomra. Egyre sürgetőbb feladat a betegek hatékony kezelése, amihez nélkülözhetetlen a betegségek kialakulásában részt vevő mechanizmusok feltárása. Jelenleg egy a közelmúltban azonosított protein neurodegenerációban betöltött szerepét vizsgálom. Habár még a munka elején járok, eredményeink igazán biztatóak, és reményeim szerint e fehérje egy új terápiás célpontként szolgálhat a jövőben.
A Neuropatológiai Kutatócsoport a neurodegeneratív betegségek mellett az agydaganatok molekuláris hátterének a feltérképezésében is aktív szerepet vállal. Erről Murnyák Balázs molekuláris biológust kérdeztük.
– Munkánk középpontjában az egyik leggyakoribb és legagresszívebb felnőttkori agydaganat, a glioblasztóma áll. A tumorokra jellemző molekuláris heterogenitás megnehezíti a diagnózisukat és a megfelelő terápia megválasztását is. Sajnos, a fejlődő terápiás eljárások ellenére, a betegség továbbra is rossz prognózisú, így a daganatkutatás egyik legsürgetőbb területét képezi. Úgy gondoljuk, hogy a hibás sejten belüli jelátviteli útvonalak vizsgálatával teljesebb képet kaphatunk az agytumorok progressziójakor bekövetkező genetikai változásokról. Munkacsoportunk Klekner Álmos idegsebész (Debreceni Egyetem Idegsebészeti Klinika) és Kálmán Bernadett neurológus (Pécsi Tudományegyetem és Szombathelyi Markusovszky Kórház) kutatócsoportjaival szoros együttműködésben olyan morfológiai, biokémiai, sejtbiológiai és neuropatológiai módszerekkel detektálható jellemzőket keres, amelyek a jövőben prognosztikai jelzést adhatnak vagy új tumorterápiás támadáspontokat határozhatnak meg. Fő célunk az agydaganatos betegek személyre szabott, hatásos kezelésének kidolgozása és megvalósítása.
 Murnyák Balázs
Murnyák BalázsPontosan milyen molekuláris eltéréseket vizsgálnak, és milyen eredményeket értek el eddig?
– Kutatócsoportunk a humán daganatokban gyakran zavart szenvedő, a p53 jelátviteli útvonal és a PARP1 DNS hibajavító fehérje kapcsolatát vizsgálja bioinformatikai, molekuláris genetikai és immunhisztokémiai módszerek alkalmazásával. Egyik kiemelkedő eredményünk, hogy elsőként írtuk le a PARP1 DNS hibajavító fehérje alcsoport-specifikus expresszióját, illetve prognosztikai szerepét a klasszikus alcsoportú glioblasztómában. Ezenfelül a TP53 mutációk egy olyan mutáció frekvencia-, illetve immunhisztokémiai jelölődésen alapuló csoportosítását határoztuk meg, amelyek hasznosak lehetnek a daganatos betegek csoportosításában, és prognosztikus relevanciával is bírnak. A témában született eredményeinket magasan jegyzett (Q1-es) nemzetközi folyóiratokban publikáltuk.
A NAP Neuropatológiai Kutatócsoport vezetőjét, Hortobágyi Tibort a korábban már említett demenciákkal kapcsolatos kutatásokról, elsősorban a Lewy-testes demenciákról kérdeztük.
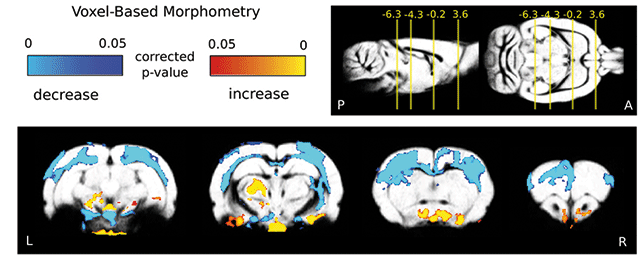
– A neurodegeneratív kórképek vonatkozásában számos alapkutatási és kliniko-patológiai vizsgálatban vezető neuropatológus hozzájárulással publikáltunk. Erre valóban egyik példa a Lewy-testes demenciák átfogó vizsgálata, szoros együttműködésben a stockholmi Karolinska Intézet és a King’s College London kutatóival. Idetartozik a klinikai diagnózis pontosságát vizsgáló munka, az „unfolded protein response” (UPR) aktiválódását Lewy-testes demenciákban igazoló publikáció, a kognitív hanyatlás klinikai és patológiai prediktív jellemzőit vizsgáló prospektív elemzés, valamint a szinaptikus fehérjék változása és a demencia összefüggéseinek analízise. Vizsgálataink a második leggyakoribb neurodegeneratív demencia vonatkozásában a klinikai progresszió fontos prediktív tényezőit határozták meg, és az idegsejtpusztulás patomechanizmusának jobb megértését tették lehetővé, lehetséges terápiás célpontok azonosításával.
 Hortobágyi Tibor
Hortobágyi TiborMilyen kutatási témákat emelne még ki?
– A Debreceni Egyetem Neurológiai Klinikája Csiba László akadémikus vezetésével a sztrók-kutatás és gyógyítás nemzetközileg is jelentős központja lett az elmúlt negyedszázadban. Az elmúlt évek neuropatológiai vonatkozású vizsgálataiban, egyebek között az érelzáródás miatt kialakuló agyi infarktust gyakran követő vérzéses átalakulást elemeztük, igazolva, hogy sokkal gyakoribb, mint klinikailag az feltételezett. A vérzéses sztrók esetén a túlélési esélyeket megadó rutin klinikai és laboradatokon alapuló értékelőrendszert dolgoztunk ki és validáltunk. A kutatási eredmények Szepesi Rita PhD-értekezésének fontos részét képezték. Emellett a vaszkuláris demencia neuropatológiai alapjait és a vaszkuláris léziók neuropatológiai pontos és egységesített meghatározását szolgáló több nemzetközi együttműködéshez járultunk hozzá. E témakört összefoglalóan jellemezve: vizsgálatainkkal az agyi érbetegségek prognózisát és klinikai tüneteit meghatározó neuropatológiai elváltozások pontosabb meghatározását értük el.•
2017. december